Abonnez-vous à notre infolettre!
Suivez les actualités de CATALIS et Recherche clinique Québec

CATALIS a développé un tableau de bord provincial PowerBI permettant d’obtenir un portrait de la recherche clinique au Québec. Accessible aux directions de recherche, cet outil offre des données standardisées qui facilitent le suivi des tendances, l’identification des enjeux et la mise en place de solutions concrètes pour améliorer la performance. Pour toute question, veuillez contacter votre centre de recherche.
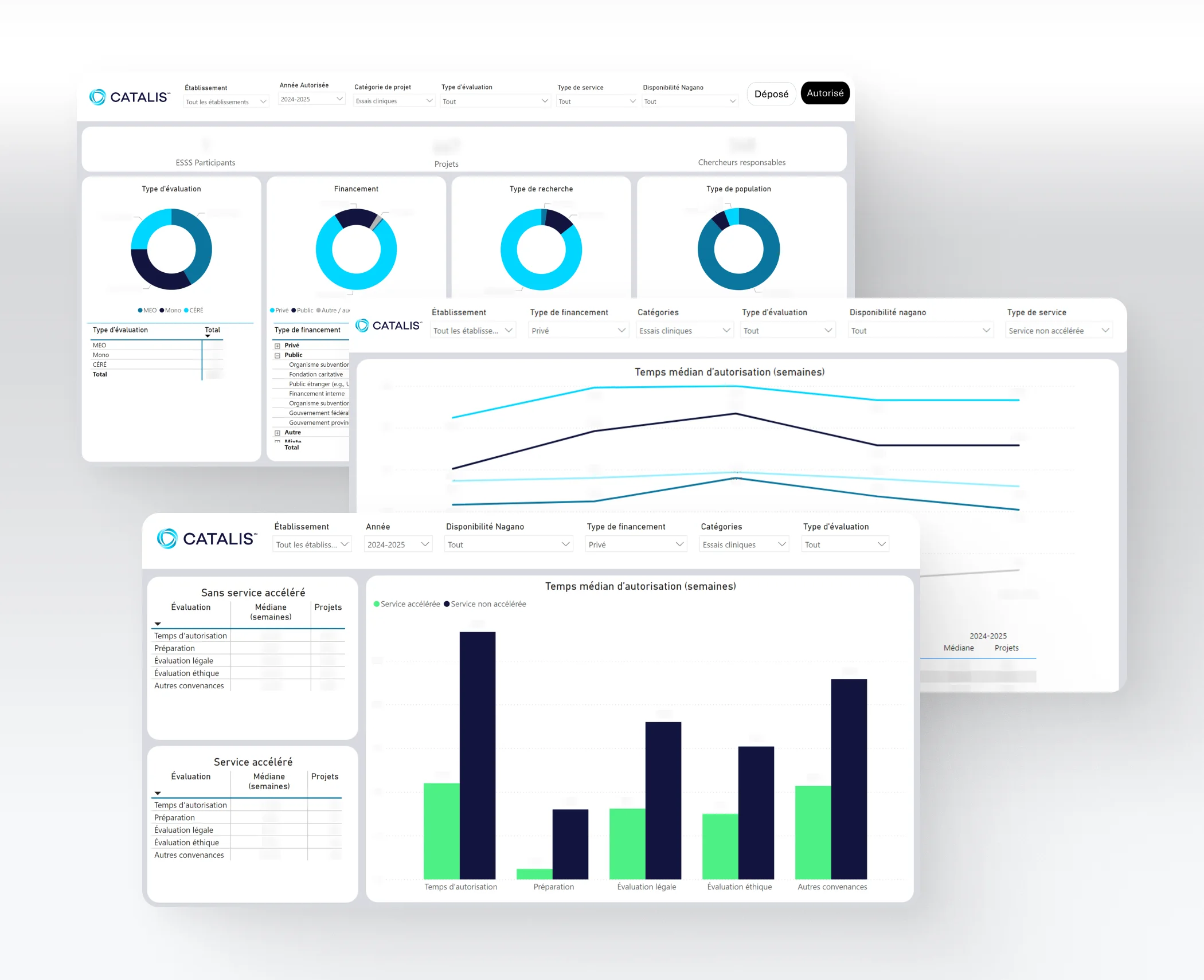
Le Service d’évaluation ACCÉLÉRÉE est une initiative unique qui positionne le Québec comme leader mondial en recherche clinique. Il vise à autoriser des essais cliniques en ≤ 8 semaines, soit une réduction de près de 75 % du temps d’autorisation standard, offrant ainsi une plus grande période pour le recrutement des participants.

Ce document donne plus de détails sur les nouveautés et les changements apportés dans la révision 3 (R3) des Bonnes pratiques cliniques (BPC) de l’International Council for Harmonisation (ICH).
Ce mémo, développé par le Réseau CATALIS, clarifie les exigences relatives à la signature du formulaire FDA1572 au Québec dans le cadre d’essais cliniques.
Ce mémo, développé par le Réseau CATALIS, clarifie les exigences canadiennes et québécoises applicables dans le cadre du Règlement (UE) n° 536/2014 en ce qui concerne la conduite d’essais cliniques au sein d’établissements du Québec.
Les clauses standardisées regroupent des informations devant figurer dans les formulaires d’information et de consentement (FIC) pour se conformer aux exigences normatives et réglementaires en vigueur au Québec lors de la conduite d’un essai clinique. Cette standardisation est issue d’un consensus des comités d’éthique de la recherche (CÉR) des établissements de Santé Québec, membres du réseau CATALIS QUÉBEC, dans le but d’assurer une cohérence décisionnelle à l’échelle du réseau.
Les autres clauses harmonisées proposent des formulations communes utilisées par des CÉR, notamment en lien avec :
Leur utilisation dans les formulaires de consentement d’essais cliniques permet de faciliter la rédaction de ces documents et d’accélérer leur approbation par les établissements du réseau de la santé et des services sociaux.
Ces MON, destinés aux membres et au personnel des CÉR, sont une adaptation québécoise du comité d’éthique du Réseau CATALIS des MON de N2 Canada. Ceux-ci sont revus par le ministère de la Santé et des Service sociaux du Québec afin d’assurer qu’ils rencontrent les exigences ministérielles.
Contenu des MON:
Cet énoncé, développé par le Réseau CATALIS et lancé par le ministère de la santé et des services sociaux, confirme les exigences réglementaires applicables dans les établissements du réseau de la santé et des services sociaux, ainsi que les nouvelles dispositions de la Charte sur la langue française.
Le Modèle provincial d’entente de confidentialité, développé par le Réseau CATALIS et lancé par le ministère de la santé et des services sociaux, est recommandé pour accélérer la signature d’une entente de confidentialité entre un promoteur et un établissement du réseau de la Santé. Si le promoteur dépose ce contrat dans sa forme originale et sans aucune modification, les établissements publics de santé du Québec l’accepteront tel quel.
Le Modèle pancanadien d’entente d’essai clinique a été développé à partir du modèle pancanadien du Canadian Clinical Trials Coordinating Centre (CCTCC) que le Réseau CATALIS a adapté au contexte réglementaire du Québec. Le mCTA provincial a été lancé par le ministère de la santé et des services sociaux afin d’accélérer la signature d’une entente d’essai clinique entre un promoteur et un établissement du réseau de la Santé. Si le promoteur dépose ce mCTA dans sa forme originale et sans aucune modification, les établissements publics de santé du Québec l’accepteront tel quel.
Ce document, élaboré par le Réseau CATALIS, définit des critères permettant de déterminer quels médicaments et procédures peuvent être considérés comme des « coûts directs de la recherche ». Il vise à soutenir les négociations budgétaires en fournissant un cadre commun d’évaluation.
Ce mémo, élaboré par le Réseau CATALIS, clarifie les responsabilités les responsabilités des parties prenantes dans le cadre d’activités menées au domicile des participants.
Ce document, élaboré par le Réseau CATALIS, précise l’impact de la fusion des établissements de santé et de services sociaux, découlant de la création de Santé Québec, sur la négociation, la conclusion et la signature de nouveaux contrats. Il clarifie également la dénomination des établissements, telle qu’approuvée par Santé Québec, laquelle doit être utilisée dans toutes les ententes conclues depuis le 1er décembre 2024.
Ce document vise à accompagner les promoteurs et les établissements du réseau de la santé et des services sociaux du Québec dans l’utilisation de logiciels et autres technologies dans les essais cliniques. Il présente les responsabilités applicables, clarifie les obligations légales et contractuelles et propose des recommandations permettant d’adapter et d’uniformiser les pratiques contractuelles.
Ce questionnaire, élaboré par le Réseau CATALIS, a été conçu pour accélérer l’autorisation d’un projet de recherche, en fournissant à la pharmacie de recherche les informations complémentaires nécessaires à l’évaluation de sa faisabilité, en plus des documents de l’étude. Il doit être rempli par le promoteur et déposé par les équipes de recherche pour évaluation par les équipes de recherche pour évaluation.
Recherche clinique Québec, propulsé par CATALIS, met à votre disposition un répertoire des établissements de santé du Québec. Cet outil facilite l’identification des sites les plus adaptés pour la réalisation d’essais cliniques précis, soutenant ainsi une recherche plus rapide, efficace et collaborative au service de la santé.
Le Registre public des essais cliniques du Québec, développé par SemiWeb via la plateforme Nagano, vous permet d’identifier les essais cliniques qui sont actuellement (ou qui ont été, ou qui seront prochainement) menés au Québec, au Canada et à travers le monde. Le Registre compile et partage, en temps réel, les données des promoteurs provenant de ClinicalTrials.gov (un registre public international) et les données des établissements publics du réseau de la santé et des services sociaux du Québec qui proviennent de la plateforme Nagano.
CATALIS s’est s’associée à N2 Canada pour offrir aux établissements de santé membres du Réseau CATALIS un accès gratuit à une plateforme commune de formation, qui vise à assurer la conduite d’une recherche de haute qualité. De plus, par l’entremise de N2 Canada, les établissements ont accès à certaines formations offertes sur la plateforme CITI-Canada (Collaborative Institutional Training Initiative).
Veuillez consulter l’offre de formation complète de N2 Canada disponible aux établissements grâce à l’association de CATALIS.
Pour accéder aux cours de N2, veuillez contacter la personne désignée comme responsable pour les accès dans votre établissement.

Ces formations, cocrées avec les membres publics et privés du comité consultatif qualité et formation de CATALIS, répondent à un besoin exprimé par les membres du Réseau : offrir des contenus courts, accessibles et engageants afin d’harmoniser les pratiques en recherche clinique. Elles sont disponibles pour les établissements sur l’environnement numérique d’apprentissage de N2. Pour accéder à ces formations, veuillez contacter la personne désignée responsable des accès à la plateforme de N2 dans votre établissement.

Cette formation présente les principes fondamentaux de la gestion des données en recherche. Elle permet de distinguer les types de données d’étude, de comprendre les notions de données sources et dérivées, ainsi que d’assurer la traçabilité ainsi que la reconstructibilité des informations. La formation aborde également les bonnes pratiques de copie de documents et le cycle de vie des documents liés à une étude.
Cette formation introduit les bonnes pratiques de documentation selon les principes ALCOA+. Le respect de ces principes contribue à assurer l’intégrité des données dans le cadre d’une étude. La formation aborde également l’application de ces principes au quotidien et la correction adéquate des documents sources en cas d’erreurs.
Cette formation explore en profondeur la délégation des tâches dans le cadre d’un protocole de recherche. Elle met en lumière l’importance d’une délégation bien structurée pour garantir la rigueur et la conformité des études cliniques, et présente les étapes clés pour l’organiser conformément aux exigences réglementaires. Parmi celles-ci : l’identification des tâches pouvant être déléguées, la sélection appropriée des membres de l’équipe appropriés, ainsi que la documentation rigoureuse de la délégation à l’aide de registres adaptés. La formation traite également de la gestion des situations particulières, telles que les changements de personnel ou les ajustements en cours d’étude. Des exemples concrets et des modèles de registres sont fournis pour faciliter la mise en pratique.
Cette formation permet de comprendre les principes de base liés à la qualité, à la conformité et à l’amélioration continue dans le cadre de la recherche.
Cet outil présenté sous forme de liste de vérification, vise à guider les établissements – notamment leur « bureau de la recherche » ou équivalent – souhaitant entreprendre des activités de recherche impliquant des participants humains, en les aidant à recenser les éléments clés de la structure administrative et logistique nécessaires pour encadrer les équipes de recherche.
Ce guide vise à aider les centres de recherche à mieux se préparer en partageant des bonnes pratiques éprouvées et en évitant les pièges courants. Conçu comme une trousse à outils, il permet de sélectionner les informations pertinentes selon vos besoins ou l’étape où vous vous trouvez. Il offre une ressource complète et pratique pour naviguer dans toutes les étapes d’une inspection, depuis la compréhension du cadre réglementaire jusqu’aux actions à entreprendre après la visite.
Télécharger la liste d’accompagnement et les annexes.
Ce guide constitue une introduction à la recherche clinique. Il est destiné à toute personne qui découvre la recherche chez l’humain, que ce soit par sa participation directe ou en tant que soutien administratif et technique. Il présente, à haut niveau, l’histoire, les différents types d’études, les concepts principaux et les rôles des différentes parties prenantes. Il est également une porte d’entrée à notre programme de recherche.
Ce cours interactif est destiné aux chercheurs qui découvrent la recherche clinique. Complément du cours « Recherche clinique 101 », il met de l’emphase sur le rôle du chercheur et les responsabilités qui lui permettront d’assurer la sécurité des participants et la conformité réglementaire des études qu’il conduira.
Ce lexique inclut des définitions provenant de sources reconnues, lesquelles sont dûment identifiées lorsque applicable. D’autres définitions y sont également proposées afin de faciliter la compréhension des différents documents et outils produits par CATALIS Québec. Ces dernières sont fournies à titre informatif uniquement et n’ont aucune valeur officielle ou normative.
Cette formation met en lumière l’importance du processus de consentement, en abordant ses dimensions historiques, réglementaires et son rôle comme processus continu centré sur l’humain. Elle explore ensuite les aspects pratiques d’une rencontre visant à obtenir le consentement, ainsi que la gestion de situations particulières.
Informations à venir.
Informations à venir.
Le Québec dispose d’un système agile et robuste d’accès aux données de santé populationnelles. Grâce à son système de santé publique universel, le Québec collecte des données massives sur la santé de la population, couvrant aussi bien les actes médicaux, que les hospitalisations, les médicaments, et les résultats d’analyses de laboratoire ou d’imagerie. Certaines données de santé anonymisées sont accessibles publiquement, tandis que d’autres doivent faire l’objet d’une demande d’accès.
L’équipe du Service d’accompagnement personnalisé de CATALIS est là pour soutenir gratuitement les patients, leurs proches aidants et les professionnels de la santé dans la recherche d’essais cliniques correspondant aux besoins et critères souhaités.
