Abonnez-vous à notre infolettre!
Suivez les actualités de CATALIS et Recherche clinique Québec

Propulsé par CATALIS Québec et appuyé par le gouvernement du Québec, le site Recherche clinique Québec est un guichet unique d’information et de soutien qui vise à fournir aux promoteurs des outils et ressources pour optimiser la planification et le déroulement de leurs projets de recherche clinique dans la province.

Ce répertoire facilite l’identification des sites les plus adaptés pour la réalisation d’essais cliniques précis, soutenant ainsi une recherche plus rapide, efficace et collaborative au service de la santé.
Ce répertoire conçu pour identifier les cliniques privées disponibles pour la réalisation de vos essais cliniques au Québec.
Ce répertoire facilite l’identification rapide de fournisseurs experts en recherche clinique et en développement biopharmaceutique partout au Québec.
Nous remercions BioQuébec pour sa précieuse collaboration dans la mise en œuvre de ce répertoire provincial.
Ce répertoire rassemble les associations de patients, les directives de traitement et les services de patients partenaires pour vous accompagner à chaque étape.
Nous remercions nos associations de patient partenaires pour leur précieuse collaboration dans l’intégration des directives de traitement à ce répertoire.
Le Registre public des essais cliniques du Québec, développé par SemiWeb via la plateforme Nagano, vous permet d’identifier les essais cliniques qui sont actuellement (ou qui ont été, ou qui seront prochainement) menés au Québec, au Canada et à travers le monde. Le Registre compile et partage, en temps réel, les données des promoteurs provenant de ClinicalTrials.gov (un registre public international) et les données des établissements publics du réseau de la santé et des services sociaux du Québec qui proviennent de la plateforme Nagano.
Le Service d’évaluation ACCÉLÉRÉE est une initiative unique qui positionne le Québec comme leader mondial en recherche clinique. Il vise à autoriser des essais cliniques en ≤ 8 semaines, soit une réduction de près de 75 % du temps d’autorisation standard, offrant ainsi une plus grande période pour le recrutement des participants.

Ce document donne plus de détails sur les nouveautés et les changements apportés dans la révision 3 (R3) des Bonnes pratiques cliniques (BPC) de l’International Council for Harmonisation (ICH).
Ce mémo, développé par le Réseau CATALIS, clarifie les exigences relatives à la signature du formulaire FDA1572 au Québec dans le cadre d’essais cliniques.
Ce mémo, développé par le Réseau CATALIS, clarifie les exigences canadiennes et québécoises applicables dans le cadre du Règlement (UE) n° 536/2014 en ce qui concerne la conduite d’essais cliniques au sein d’établissements du Québec.
Les clauses standardisées regroupent des informations devant figurer dans les formulaires d’information et de consentement (FIC) pour se conformer aux exigences normatives et réglementaires en vigueur au Québec lors de la conduite d’un essai clinique. Cette standardisation est issue d’un consensus des comités d’éthique de la recherche (CÉR) des établissements de Santé Québec, membres du réseau CATALIS QUÉBEC, dans le but d’assurer une cohérence décisionnelle à l’échelle du réseau.
Les autres clauses harmonisées proposent des formulations communes utilisées par des CÉR, notamment en lien avec :
Leur utilisation dans les formulaires de consentement d’essais cliniques permet de faciliter la rédaction de ces documents et d’accélérer leur approbation par les établissements du réseau de la santé et des services sociaux.
Cet énoncé, développé par le Réseau CATALIS et lancé par le ministère de la santé et des services sociaux, confirme les exigences réglementaires applicables dans les établissements du réseau de la santé et des services sociaux, ainsi que les nouvelles dispositions de la Charte sur la langue française.
Le Modèle provincial d’entente de confidentialité, développé par le Réseau CATALIS et lancé par le ministère de la santé et des services sociaux, est recommandé pour accélérer la signature d’une entente de confidentialité entre un promoteur et un établissement du réseau de la Santé. Si le promoteur dépose ce contrat dans sa forme originale et sans aucune modification, les établissements publics de santé du Québec l’accepteront tel quel.
Le Modèle pancanadien d’entente d’essai clinique a été développé à partir du modèle pancanadien du Canadian Clinical Trials Coordinating Centre (CCTCC) que le Réseau CATALIS a adapté au contexte réglementaire du Québec. Le mCTA provincial a été lancé par le ministère de la santé et des services sociaux afin d’accélérer la signature d’une entente d’essai clinique entre un promoteur et un établissement du réseau de la Santé. Si le promoteur dépose ce mCTA dans sa forme originale et sans aucune modification, les établissements publics de santé du Québec l’accepteront tel quel.
Ce document, élaboré par le Réseau CATALIS, définit des critères permettant de déterminer quels médicaments et procédures peuvent être considérés comme des « coûts directs de la recherche ». Il vise à soutenir les négociations budgétaires en fournissant un cadre commun d’évaluation.
Ce mémo, élaboré par le Réseau CATALIS, clarifie les responsabilités les responsabilités des parties prenantes dans le cadre d’activités menées au domicile des participants.
Ce document, élaboré par le Réseau CATALIS, précise l’impact de la fusion des établissements de santé et de services sociaux, découlant de la création de Santé Québec, sur la négociation, la conclusion et la signature de nouveaux contrats. Il clarifie également la dénomination des établissements, telle qu’approuvée par Santé Québec, laquelle doit être utilisée dans toutes les ententes conclues depuis le 1er décembre 2024.
Ce document vise à accompagner les promoteurs et les établissements du réseau de la santé et des services sociaux du Québec dans l’utilisation de logiciels et autres technologies dans les essais cliniques. Il présente les responsabilités applicables, clarifie les obligations légales et contractuelles et propose des recommandations permettant d’adapter et d’uniformiser les pratiques contractuelles.
Ce questionnaire, élaboré par le Réseau CATALIS, a été conçu pour accélérer l’autorisation d’un projet de recherche, en fournissant à la pharmacie de recherche les informations complémentaires nécessaires à l’évaluation de sa faisabilité, en plus des documents de l’étude. Il doit être rempli par le promoteur et déposé par les équipes de recherche pour évaluation par les équipes de recherche pour évaluation.
Saviez-vous que les établissements de santé du Québec ont accès à de nombreuses formations offertes par N2?

Saviez-vous que les établissements de santé du Québec ont accès à de nombreuses formations offertes par Recherche clinique Québec?

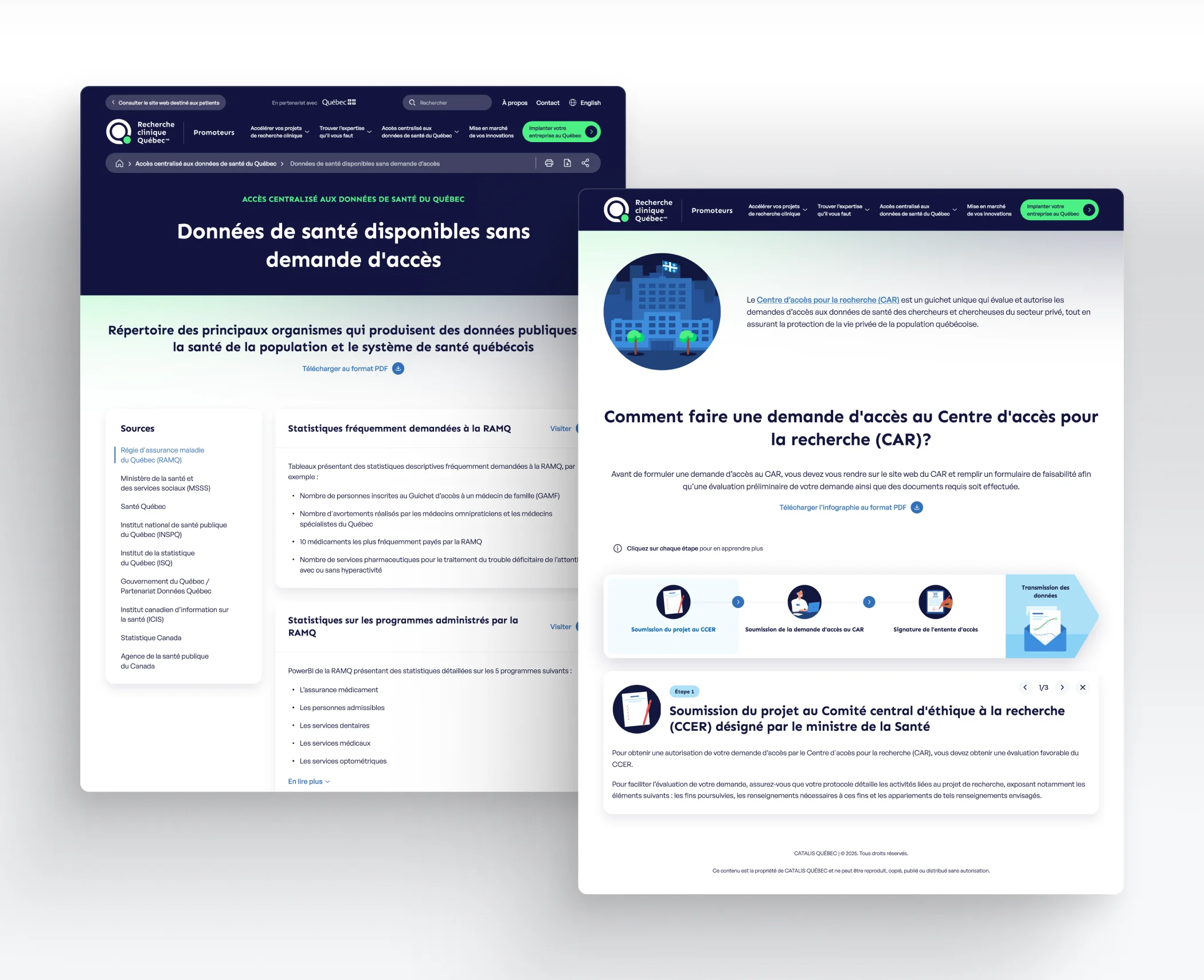
Grâce à son système de santé publique universel, le Québec collecte des données massives sur la santé de la population, couvrant aussi bien les actes médicaux, que les hospitalisations, les médicaments, et les résultats d’analyses de laboratoire ou d’imagerie. Certaines données de santé anonymisées sont accessibles publiquement, tandis que d’autres doivent faire l’objet d’une demande d’accès.
Sept des dix plus grandes entreprises pharmaceutiques mondiales – notamment AbbVie, Pfizer, Merck, Novartis, Roche, GSK et Bristol Myers Squibb – y ont établi leurs activités, témoignant de l’excellence de son environnement d’affaires et de la force de son maillage entre industrie, recherche et innovation.
